
扫码体验VIP

扫码VIP小程序
系统提示:股票复盘网只提供基本的股票信息,如果需要了解实时、详细的股票行情数据,请登录VIP复盘网..
|
恒瑞医药
600276 |
2.99%
|
最新:56.58
开盘:55.3 昨收:54.94 |
开盘%:0.66%
振幅%:2.64% 换手%:0.72% |
最高:56.75
最低:55.3 量比:0.9 |
总市值:3755 亿
流通值:3609 亿 成交额:64 亿 |
- 基本信息
- 主力分时图 New
- 股票百科
- 个股快讯
- 上市公司
- 更多股票
- 专家分析
- 龙虎榜
- 历史涨停原因
- 董秘互动
- 分时图
- 日K图
- 周K图
- 月K图
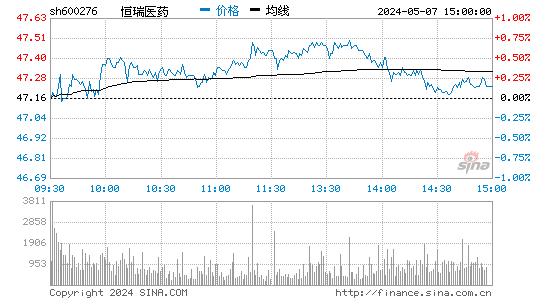
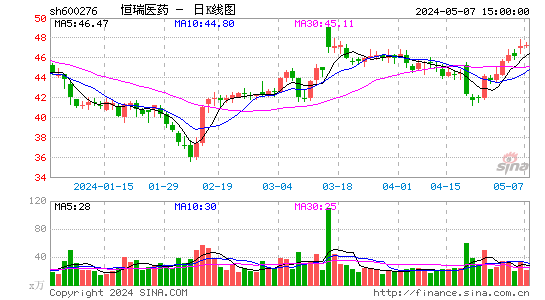
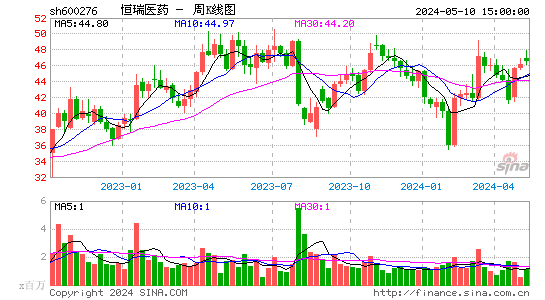
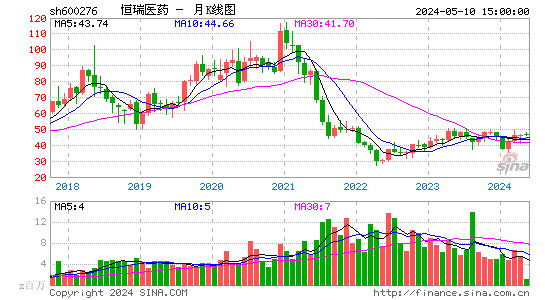
恒瑞医药股票概览
了解恒瑞医药及其股票投资价值
公司概况
恒瑞医药是一家专注于医药创新和高质量发展的公司,致力于提供优质的医药产品和服务。公司拥有强大的研发团队和先进的技术平台,不断推动医药领域的创新和发展。
业务领域
研发创新:恒瑞医药在抗肿瘤、麻醉、抗感染等多个领域拥有领先的产品线,并持续投入研发,拓展新的治疗领域。
市场营销:公司拥有完善的营销网络和专业的销售团队,能够迅速将创新产品推向市场,满足患者需求。
国际合作:恒瑞医药积极拓展国际市场,与国际知名药企开展合作,提升公司的全球竞争力。
财务表现
近年来,恒瑞医药的财务表现稳健。公司营收持续增长,净利润水平保持在较高水平。同时,公司的研发投入也在不断增加,为公司的长期发展提供了有力保障。
股票投资价值
作为医药行业的佼佼者,恒瑞医药的股票具有较高的投资价值。公司的创新能力和稳健的财务表现使其成为众多投资者的优选。然而,股票投资存在风险,投资者需结合自身风险承受能力进行决策。
总结
恒瑞医药是一家具有创新精神和稳健财务表现的医药公司。其业务领域广泛,研发实力强大,股票具有较高的投资价值。关键词:恒瑞医药、股票、投资价值。
以上是对恒瑞医药及其股票的全面介绍,希望能够帮助投资者更好地了解这家公司和其股票的投资价值。
2026-03-09 17:23
【恒瑞医药:子公司收到HRS9531注射液药物临床试验批准通知书】3月9日电,恒瑞医药(600276.SH)公告称,公司子公司福建盛迪医药有限公司收到国家药监局核准签发的HRS9531注射液的《药物临床试验批准通知书》,将于近期开展临床试验。HRS9531注射液是一种新型靶向抑胃肽受体(GIPR)和胰高血糖素样肽-1受体(GLP-1R)的双激动剂,针对慢性肾脏病(CKD)适应症,全球范围内暂无同类药物获批上市。截至目前,HRS9531相关项目累计研发投入约6.32亿元。根据相关法律法规要求,药物在获得药物临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2026-03-06 17:06
【恒瑞医药:子公司收到阿得贝利单抗注射液和SHR-8068注射液的药物临床试验批准通知书】3月6日电,恒瑞医药(600276.SH)公告称,子公司苏州盛迪亚生物医药有限公司、上海盛迪医药有限公司收到国家药品监督管理局核准签发关于阿得贝利单抗注射液、SHR-8068注射液的《药物临床试验批准通知书》,将于近期开展临床试验。阿得贝利单抗注射液是公司自主研发的人源化抗PD-L1单克隆抗体,SHR-8068注射液是公司引进的一款全人源抗CTLA-4单克隆抗体。根据我国药品注册相关的法律法规要求,药物在获得药物临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2026-03-06 17:06
【恒瑞医药:子公司收到阿得贝利单抗注射液药物临床试验批准通知书】3月6日电,恒瑞医药(600276.SH)公告称,公司子公司上海盛迪医药有限公司收到国家药监局核准签发关于阿得贝利单抗注射液的《药物临床试验批准通知书》,将于近期开展临床试验。该药物为公司自主研发的人源化抗PD-L1单克隆抗体,拟用于可切除胃癌或胃食管结合部癌围手术期治疗的随机、双盲、多中心III期临床研究。根据相关法律法规要求,药物在获得药物临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2026-03-06 10:11
【港股医药股持续走高,三生制药涨超8%】港股医药股持续走高,三生制药涨超8%,恒瑞医药涨超5%,复星医药、中国生物制药、石药集团纷纷拉升。
2026-03-04 17:06
【恒瑞医药:子公司收到HRS-1780片药物临床试验批准通知书】3月4日电,恒瑞医药(600276.SH)公告称,公司子公司山东盛迪医药有限公司收到国家药监局核准签发的HRS-1780片的《药物临床试验批准通知书》,同意开展用于治疗原发性醛固酮增多症的临床试验。HRS-1780片是盐皮质激素受体拮抗剂,截至目前,相关项目累计研发投入约为7,040万元。根据相关法律法规要求,药物在获得药物临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2026-03-04 17:05
【恒瑞医药:子公司收到药物临床试验批准通知书】3月4日电,恒瑞医药(600276.SH)公告称,公司子公司苏州盛迪亚生物医药有限公司、上海恒瑞医药有限公司收到国家药监局核准签发关于注射用SHR-A2102、SHR-8068注射液的《药物临床试验批准通知书》,将于近期开展临床试验。注射用SHR-A2102为靶向Nectin-4的抗体药物偶联物(ADC),SHR-8068注射液为全人源抗CTLA-4单克隆抗体。根据相关法律法规,药物在获得药物临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2026-02-24 16:37
恒瑞医药:SHR-1918注射液药品上市许可申请获受理并纳入优先审评程序。
2026-02-11 16:54
【恒瑞医药:注射用瑞康曲妥珠单抗纳入突破性治疗品种名单】2月11日电,恒瑞医药(600276.SH)公告称,公司子公司苏州盛迪亚生物医药有限公司的注射用瑞康曲妥珠单抗被国家药品监督管理局药品审评中心纳入突破性治疗品种名单,这是该药品第10项获得突破性治疗认证的适应症。该药品拟定适应症为HER2(ERBB2)激活突变的局部晚期或转移性非小细胞肺癌患者的一线治疗。
2026-02-10 20:24
【恒瑞医药:瑞普泊肽片中国Ⅱ期减重研究取得积极顶线数据】2月10日,恒瑞医药与美国Kailera Therapeutics公司(Kailera)共同宣布,GLP-1/GIP双重受体激动剂——每日一次口服瑞普泊肽片(也称HRS9531片、KAI-9531-T)在中国166名肥胖成人中开展的Ⅱ期临床试验(NCT06841445)取得积极顶线数据。基于假想策略的估计目标分析结果显示,瑞普泊肽片治疗第26周时,参与者较基线平均体重下降最高达12.1%,且未观察到平台期,同时呕吐发生率不超过11.4%。恒瑞医药计划在中国推进瑞普泊肽片治疗肥胖症的Ⅲ期临床试验,Kailera计划于2026年启动全球Ⅱ期临床试验。此外,瑞普泊肽也正在开发皮下注射疗法。
2026-02-06 16:35
【恒瑞医药:HRS-4642注射液纳入突破性治疗品种名单 目前国内外尚无同类药物获批上市】2月6日电,恒瑞医药(600276.SH)公告称,公司的HRS-4642注射液被国家药品监督管理局药品审评中心纳入突破性治疗品种名单,拟定适应症为联合吉西他滨和紫杉醇(白蛋白结合型)用于携带KRAS G12D突变的晚期或转移性胰腺癌的一线治疗。截至目前,相关项目累计研发投入约2.54亿元。经查询,目前国内外尚无同类药物获批上市。
2026-02-05 16:50
【恒瑞医药:SHR-1894注射液药物临床试验获批】2月5日电,恒瑞医药(600276)2月5日公告,公司子公司苏州盛迪亚生物医药有限公司收到国家药监局核准签发关于SHR-1894注射液的《药物临床试验批准通知书》,将于近期开展临床试验。SHR-1894注射液是公司自主研发的一种治疗用生物制品,预期可在特应性皮炎治疗过程中,发挥保护皮肤屏障和抑制炎症的作用。此外,公司收到国家药监局下发的《受理通知书》,公司HR091506片的上市许可申请获国家药监局受理。HR091506 片拟定用于痛风患者高尿酸血症的长期治疗。
2026-02-05 16:40
【恒瑞医药:HR091506片上市许可申请获国家药监局受理】2月5日电,恒瑞医药(600276.SH)公告称,公司HR091506片的上市许可申请获国家药监局受理。该药品拟定适应症为用于痛风患者高尿酸血症的长期治疗。此次申报上市基于两项随机、双盲、非布司他片阳性对照的关键Ⅲ期临床研究,结果显示HR091506片在主要终点上均显著优于试验对照组,且安全性良好。HR091506片是恒瑞医药采用胃滞留制剂技术自主研发的具有脉冲释放特性的非布司他口服缓释片剂,截至目前累计研发投入约1.27亿元。
2026-02-05 16:40
【恒瑞医药:子公司收到SHR-1894注射液临床试验批准通知书】2月5日电,恒瑞医药(600276.SH)公告称,子公司苏州盛迪亚生物医药有限公司收到国家药品监督管理局核准签发的关于SHR-1894注射液的《药物临床试验批准通知书》,将于近期开展临床试验。SHR-1894注射液是公司自主研发的一种治疗用生物制品,预期可在特应性皮炎治疗过程中发挥保护皮肤屏障和抑制炎症的作用。截至目前,该项目累计研发投入约为4010万元。根据相关法律法规要求,药物在获得药物临床试验批准通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
2026-02-02 16:31
恒瑞医药:重新提交注射用卡瑞利珠单抗的生物制品许可申请获FDA受理。
2026-01-30 16:49
恒瑞医药:注射用磷罗拉匹坦帕洛诺司琼的药品上市许可申请获受理。
2026-01-29 16:39
恒瑞医药:公司创新药注射用卡瑞利珠单抗联合甲磺酸阿帕替尼片新适应症的上市许可申请获受理。
2026-01-29 16:38
恒瑞医药:HRS-7535片获得药物临床试验批准通知书。
2026-01-28 14:35
【恒瑞医药口服小分子GLP-1R激动剂用于高血压合并超重或肥胖获批Ⅲ期临床】1月28日,恒瑞医药宣布,子公司山东盛迪医药有限公司收到国家药品监督管理局核准签发的《药品临床试验批准通知书》,同意公司自主研发的1类创新口服小分子GLP-1受体激动剂HRS-7535片开展用于高血压合并超重或肥胖适应症的Ⅲ期临床研究。HRS-7535片是一种新型口服小分子GLP-1R激动剂,目前全球范围内尚无口服小分子GLP-1R激动剂上市。
2026-01-27 19:46
【恒瑞医药:HRS-5346片被纳入突破性治疗品种名单】1月27日电,恒瑞医药(600276)1月27日公告,近日,子公司山东盛迪医药有限公司的HRS-5346片被国家药品监督管理局药品审评中心纳入突破性治疗品种名单。该药品拟定适应症(或功能主治):用于治疗脂蛋白(a)水平的升高。经查询,目前国内外尚无同类产品获批上市。
2026-01-27 16:49
【恒瑞医药:已回购907.37万股,使用资金总额6.05亿元】恒瑞医药1月27日公告,公司于2025年8月20日召开第九 届董事会第十八次会议审议通过了《关于以集中竞价交易方式回购公司A股股份 方案的议案》,同意公司使用自有资金,以集中竞价交易方式回购公司股份用于实 施A股员工持股计划。回购价格不超过90.85元/股(含),回购资金总额不低于10亿元且不超过20亿元。回购期限为自董事会审议通过回购股份 方案之日起12个月以内。截至2026年1月27日,公司累计回购907.37万股,占公司总股本的0.14%,回购价格区间为57.2元/股至70元/股,累计使用资金6.05亿元(不含交易费用)。
2026-01-27 16:47
【恒瑞医药:子公司HRS-5346片被纳入突破性治疗品种名单】1月27日电,恒瑞医药(600276.SH)公告称,公司子公司山东盛迪医药的HRS-5346片被国家药品监督管理局药品审评中心纳入突破性治疗品种名单。该药物用于治疗脂蛋白(a)水平的升高,目前国内外尚无同类产品获批上市。截至目前,HRS-5346片相关项目累计研发投入约为7,630万元。药品研发存在技术、审批、政策等多方面因素的影响,审评政策及未来药品市场竞争形势等存在不确定性风险。
2026-01-27 16:47
【恒瑞医药:子公司HRS-5346片被纳入突破性治疗品种名单】1月27日电,恒瑞医药(600276.SH)公告称,公司子公司山东盛迪医药的HRS-5346片被国家药品监督管理局药品审评中心纳入突破性治疗品种名单。该药物用于治疗脂蛋白(a)水平的升高,目前国内外尚无同类产品获批上市。截至目前,HRS-5346片相关项目累计研发投入约为7,630万元。药品研发存在技术、审批、政策等多方面因素的影响,审评政策及未来药品市场竞争形势等存在不确定性风险。
2026-01-26 16:41
恒瑞医药:获得SHR-1049注射液药物临床试验批准通知书。
-
VIP复盘工具
- 更多复盘工具
- 股票复盘百科
-
股票复盘知识
- 提高信息判断力:投资者如何在复杂市场中理性利用“风声”
- 股市迷雾中的灯塔:探寻与把握“确定性”投资机会
- CCI指标:短线交易的精准导航仪
- 揭秘股票快速升涨的核心要素
- 股市生存法则:揭秘北京炒家的三大盈利路径
- 波段操作:如何巧妙利用股票调整期获利
- 塑造炒股高手的必备心态与路径
- 股市弹坑理论:精准抄底的智慧策略
- 突发消息下的选股策略
- 十字星研判:解锁市场趋势与心理变化的钥匙
- 震荡上行中的智慧抉择:精准捕捉买入点策略
- 揭秘股神绝技:集合竞价选股策略深度剖析
- 熊市中的长线投资智慧:稳健选股,持续增值
- 揭秘股市智慧:“跌减涨增量”策略实战解析
- 股市生存法则:深刻理解止损的重要性与策略
- 揭秘股市奇才的选股策略:趋势、技巧与心态的三重奏
- 题材股炒作攻略:六步制胜法则
- 结构性行情下的题材股操作策略:捕捉机遇,规避风险
- 大买单与主力的识别及应对策略
- MACD“山下山”形态:精准把握股市清仓时机
当前版本:V3.0

 VIP复盘网
VIP复盘网
